Estudo revela mecanismo pelo qual o ácido úrico causa dano vascular
Agência FAPESP * – Cientistas do Centro de Pesquisa em Processos Redox em Biomedicina (Redoxoma), um Centro de Pesquisa, Inovação e Difusão (CEPID) financiado pela FAPESP e sediado no Instituto de Química (IQ) da Universidade de São Paulo (USP), propõem um mecanismo para explicar como o ácido úrico causa lesões vasculares que podem levar a doenças cardiovasculares.
O ácido úrico, um metabólito abundante no plasma humano, é propenso à oxidação em condições inflamatórias. A oxidação do ácido úrico está associada a doenças cardiovasculares, por induzir disfunção endotelial, estresse oxidativo e inflamação sistêmica e local.
Os vasos sanguíneos são revestidos pelo endotélio, que tem funções complexas para a manutenção da homeostase vascular, como regulação do fluxo sanguíneo, da coagulação, da proliferação de células da parede vascular e de respostas inflamatórias e imunológicas. O endotélio expressa uma enzima chamada peroxidasina, que é essencial para a sobrevivência das células endoteliais e, principalmente, para a estruturação da matriz extracelular, o conjunto de moléculas que une e fixa as células para formar os tecidos.
Os pesquisadores do Redoxoma mostraram que o ácido úrico é oxidado pela peroxidasina em células endoteliais, prejudicando a formação da matriz extracelular e causando a diminuição da adesão e migração dessas células.
O resultado do estudo foi publicado em artigo na revista científica Antioxidants. Os cientistas foram liderados pela professora Flavia Meotti, do IQ-USP, e tiveram apoio da FAPESP.
Em entrevista para a Assessoria de Imprensa do Redoxoma, Meotti explicou que os resultados do estudo elucidam tanto o papel do ácido úrico na disfunção endotelial quanto as funções da peroxidasina. “Como a peroxidasina é uma enzima que foi descrita recentemente, todos esses achados sobre ela são relevantes para entendermos de fato o que ela está fazendo e como a reatividade dela pode modificar a função endotelial”, pontua.
Peroxidasina
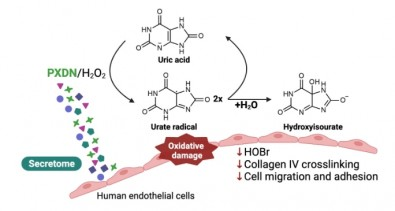
Peroxidases são enzimas que oxidam substratos na presença do peróxido de hidrogênio. O grupo de Meotti já havia mostrado em estudos anteriores que o ácido úrico é oxidado pela mieloperoxidase, gerando o radical livre de urato e hidroperóxido de urato, ambos capazes de causar danos oxidativos.
Com o objetivo de investigar se o ácido úrico reage com a peroxidasina e compromete a função da enzima nas células endoteliais humanas, o primeiro passo do estudo foi encontrar a peroxidasina no secretoma de células endoteliais vasculares (HUVEC). O secretoma é um conjunto de proteínas secretadas. Para encontrá-la, os pesquisadores fizeram uma análise proteômica. “Usamos células endoteliais para mostrar a relevância fisiológica do processo”, afirma Meotti.
Depois, analisando células HEK293 que superexpressam a enzima, os pesquisadores confirmaram que a peroxidasina oxida o ácido úrico. E, por fim, estudaram células PFHR9, que superproduzem matriz extracelular. “Queríamos extrair a matriz para poder ver o efeito do ácido úrico sobre ela”, comenta a professora. Os resultados mostraram a diminuição da formação das ligações cruzadas do colágeno IV na matriz extracelular.
Ao investigar a função celular das células endoteliais, os pesquisadores observaram que tanto o ácido úrico quanto um inibidor da peroxidasina, o floroglucinol, prejudicam os processos de adesão e migração das células. O mesmo processo também é observado em células nas quais a inserção de um RNA de interferência impede a expressão da enzima.
Com isso, o grupo do Redoxoma comprovou que adesão e migração são dependentes da peroxidasina e que o efeito do ácido úrico nesses processos também está relacionado à inibição da enzima.
Adesão e migração são essenciais para o reparo tecidual, angiogênese e manutenção da integridade vascular. Segundo Meotti, esses processos funcionais são importantes, por exemplo, na regeneração de um vaso. “Quando você tem aterosclerose, o vaso é lesionado pelo processo inflamatório, pelas espécies oxidantes que são formadas, e o processo de adesão e migração colaboram com a cicatrização, ajudando o vaso a se recuperar. Então, se você prejudica isso também, é mais um mecanismo que impede a solução da lesão.”
A pesquisa foi realizada durante o doutorado de Bianca Dempsey e o pós-doutorado de Litiele Cezar Cruz, ambas bolsistas da FAPESP e primeiras autoras do artigo.
*Com informações da Assessoria de Imprensa do Redoxoma.





Comentários